BEACON碧康制药
由欧洲财团参与投资,南亚地区唯一执行欧盟技术规范的上市制药企业,产品符合欧洲药典和美国药典标准。

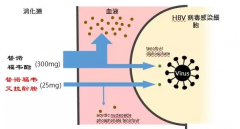
由美国制药巨头吉利德(Gilead)开发的抗病毒药物Vemlidy(Tenofovir Alafenamide,TAF,25mg)在上月获得美国FDA批准,用于慢性乙型肝炎患者的治疗。几乎在同一时间,Vemlidy(TAF)也获得欧洲药品管理局(EMA)人用医药产品委员会(CHMP)支持批准的积极意见;欧盟委员会(EC)在做出最终审查决定时通常都会采纳CHMP的建议,这也意味着Vemlidy(TAF)极有可能在未来2-3个月获批上市,造福欧洲的乙肝患者。就在最近,Vemlidy(TAF)在亚洲监管方面也传来了喜讯,日本卫生劳动福利部(MHLW)已批准Vemlidy用于慢性乙型肝炎患者,具体适用人群为存在乙肝病毒复制证据且肝功能异常的患者。
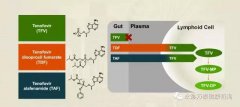
Vemlidy(TAF,替诺福韦艾拉酚胺富马酸)是一种新型核苷类逆转录酶抑制剂(NRTI),该药是已上市药物Viread(替诺福韦酯,TDF,在日本由葛兰素史克销售)的升级版。在临床试验中,TAF已被证明在低于Viread十分之一剂量时,就具有非常高的抗病毒疗效,同时具有更好的安全性,可改善肾功能和骨骼安全参数。